Twitter@YaUsGfcqxuo2ffx)です

今日は中学校理科の水にとける物質の取り出す方法について学んでいくよ

取り出せるの?

いろいろな実験が出てくるので見ていこう

はい!
水に溶ける物質の溶け方と取り出し方
前回の記事
これだけ覚えて点数アップ!中学1年理科8水溶液の性質と質量パーセントの求め方テスト対策問題
水に溶けている物質を取り出す実験方法はテストでも必ずと言っていいほど出題されるので
しっかりとどのような実験でどうやって取り出すことができるかを頭にいれてテスト対策していこう
ここではろ過の方法や手順を見ていくよ
最終的には実験の方法と結果を答えられるようになればOK
水に溶ける物質の取り出し方
- 水に溶ける物質の特徴
→最初にこの単元で出てくる用語の確認をしていこう- 結晶
→いくつかの平面に囲まれた、規則正しい形をした固体。
結晶の形は物質によって決まっているよ
【結晶の作り方】
①高温にして、とけるだけとかす
②温度を下げていくと、とけきれない分が固体(結晶)となってててくるよ。
水にとけやすい物質ととけにくい物質
→多くの物質は、水にいくらでもとけるわけでなくて水にとける量には限度がある
これを利用していくんだよ - 飽和水溶液
→物質がそれ以上溶けることができなくなった水溶液のことだよ - 溶解度
→物質が水100gにどれだけとけるかを表した数値のことだよ
溶解度は温度によって違う
=溶解度は温度が高いほど大きいよ
お茶やココアを入れるときにぬるいお水よ熱いお茶の方が溶けるよね(イメージ)
(例)砂糖の溶解度は60°Cで287g、100°Cで485g
食塩は例外で、温度によってあまり変わらないという性質があるよ
ここは下でグラフを見ながら解説するから安心して - 硝酸カリウムの溶解度
→高い温度の水にとける量と、低い温度にとける量の差が大きいので、高い温度の飽和水溶液の温度を下げると硝酸カリウムが大量の結晶となって出てくる
=食塩は温度を上げても下げても溶ける量にはほとんど変化ないけれど硝酸カリウムは温度によって変化があることをおさえておこう
=飽和水溶液の温度を下げても、食塩から結晶は少ししか出てこないよ - 再結晶
→固体の物質をいったん水にとかし、溶解度の差を利用して、再び結晶としてとり出すことだよ
【簡単な例題】
今、100g、60°Cの水に、硝酸カリウムをとるだけ入れて、飽和水溶液をつくった。
そのまま置いておくと温度が40°cになった。どんなことが起こる?? - 塩化ナトリウム
→ちなみに理科では食塩のことを塩化ナトリウムというので覚えておこう
- 結晶
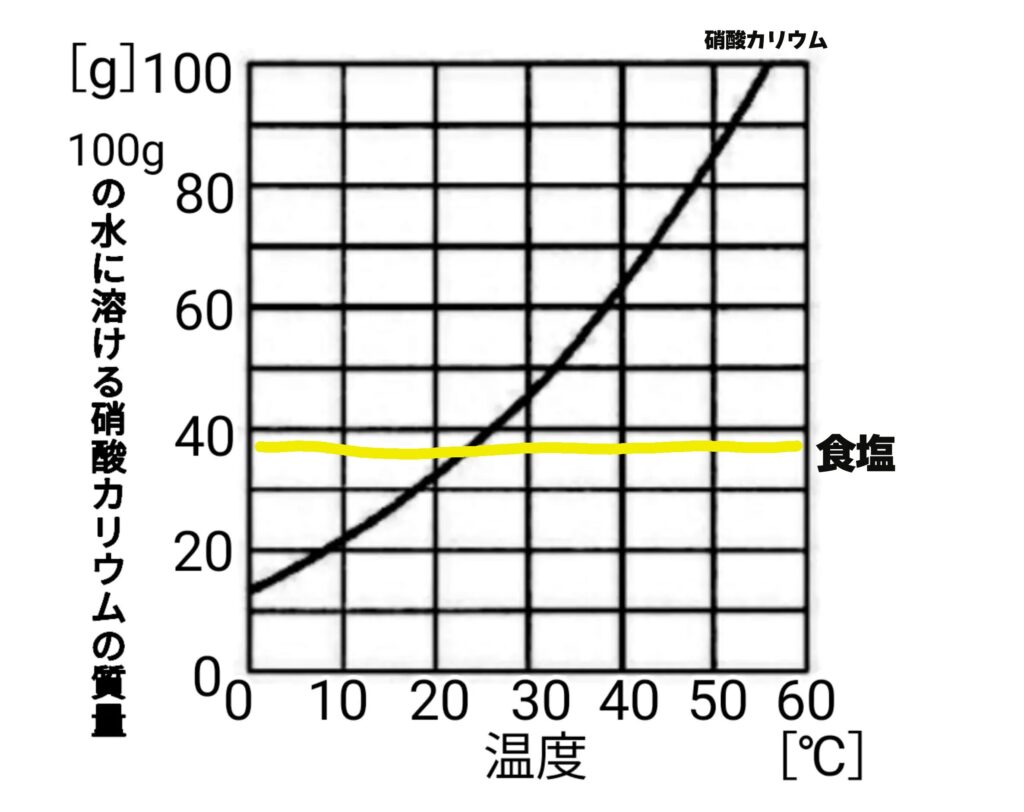
これは溶解度曲線のグラフだよ
今回は食塩と硝酸カリウムの2つを例に見ていくよ
(ミョウバンの場合もあるので復習する時はミョウバンも見てね)
縦線は100gの水に対してこれだけ溶けることができたよというもの
横線は温度だね
ということは硝酸カリウムが温度が上がれば上がるほどどうなるかというと溶けるというのがわかるよね
10℃の時は20くらいしか溶けなかったのに50℃を超えるとほぼ全部溶けてるよね!
ただし食塩はどうなっている?かというと
温度を上げても38gくらいしか溶けてないよね?
では問題として温度が40℃の時食塩と硝酸カリウムはどれくらい溶けている?
食塩→38gくらい
硝酸カリウム→60gくらい
だね
この状態から温度を10℃まで冷やすとどうなるか
ポイントは溶解度は温度が高いほど大きい
なので10℃まで下げてしまうと
食塩には変化がないけど、硝酸カリウムは10℃になると
21gくらいになってるよね
60gあったのが21gになってるこの差が結晶となるということをイメージしておこう
これが溶解度曲線の考え方だよ!
よって結晶がたくさん出てくるのは硝酸カリウムだね
=差が少ない食塩は結晶が出にくいんだよ
記事のまとめ
- 温めてから冷やした時の差が結晶として出るイメージを持っておこう
- 溶解度曲線の見方を必ず覚えよう
ろ過のやり方
- ろ過
→紙などを使って、液体のなかに混ざっている固体を液体から取り出す方法
ここではろ過の実験方法などを覚えていこう - ろ過するときの注意点
- ろ過するときの注意点
- 液はガラス棒を伝わらせて入れ、ろ紙の8分目以上入れないようにする
- ガラス棒はろ紙が重なっているところに当てる。
- ろうとのあしは、ビーカーの壁につける
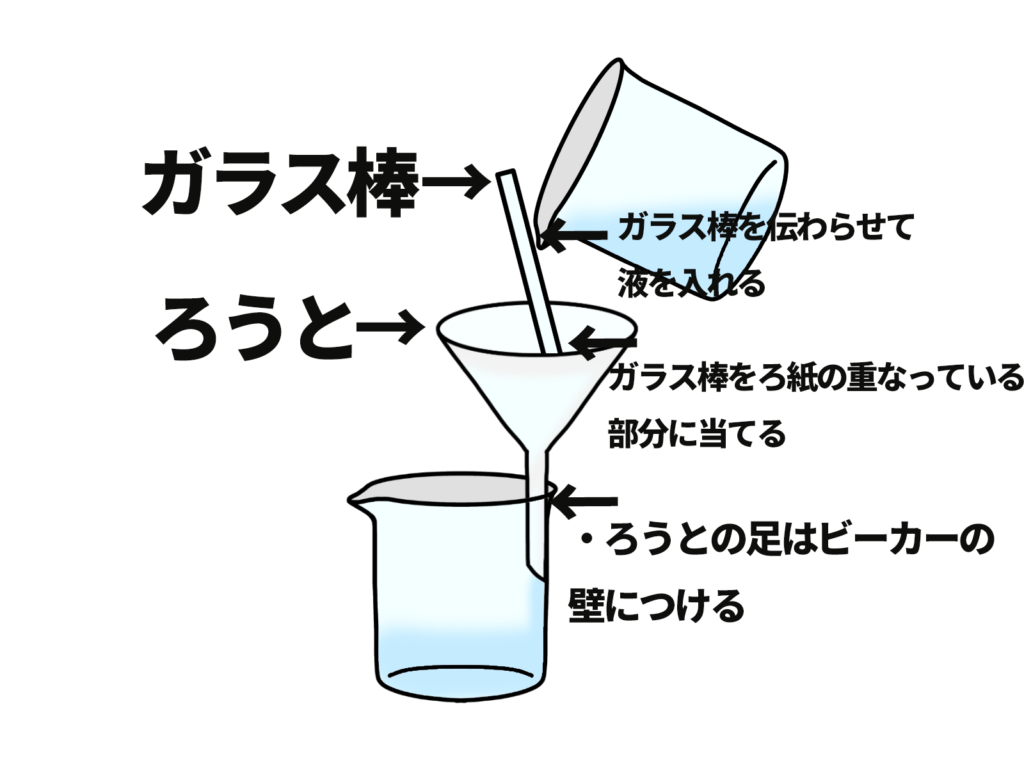
上の文章を図で説明しているので確認しておいてね
記事のまとめ
- デンプンのろ過はよくテストに出るので何が残るか覚えておこう
- ろ過の基本的な手順は答えられるように
デンプンのろ過
- 実験
→デンプンのろ過を実際に見てみよう - 水50cmに、デンプンを薬品さじ1杯、それぞれ別々に入れよくかきまぜる。どんな様子になるか見ていこう
→デンプンは白くにごるよ、透明ではないね - この液体をろ過してしばらくそのまま放置するとどうなるか
→ろ紙にはデンプン(粉)が残る
デンプンはろ紙より大きいのでろ紙を通り抜けずろ紙に残るよ - ろ紙を通った液体はどうなるか?
→水になる - ろうとのあしは、ビーカーの壁につける
| 水に物質が溶ける場合 | 水に物質が溶けない場合 | |
|---|---|---|
| よくかき混ぜる | 透明になる | 白くにごる |
| しばらく放置 | 透明のまま | 下に沈む |
| ろ過すると | 何も残らない | デンプンがろ紙に残り ろ紙を通った後のものは水になる |
中学理科テスト対策問題
- 一定量の水(ふつう100g)に溶ける物質の最大の量を何というか答えよう
↓解答解説↓
答え→溶解度 - 物質が(1)まで溶けた状態の水溶液を何というか答えよう。
↓解答解説↓
答え→飽和水溶液 - 水の温度と、溶解度の関係を表すグラフを何というかう。
↓解答解説↓
答え→溶解度曲線 - 規則正しい形の固体を何というか答えよう
↓解答解説↓
答え→結晶 - 固体を水に溶かし、溶解度の差を利用して、特び結晶として取り出すことを何というか答えよう
↓解答解説↓
答え→再結晶 - 5の方法で取り出した物質は純粋な物質と混合物どちらか答えよう
↓解答解説↓
答え→純粋物な物質
中学理科定期テストレベルテスト対策問題
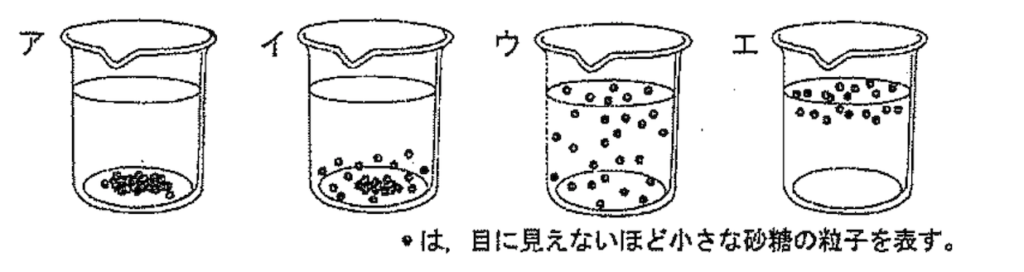
[実験1]
ビーカーに入れた水に砂糖を入れてよくかきまぜたところ、砂糖はすべてとけた。このときできた砂糖水を、3日間そのままにしておいた。
[実験2]
デンプンが砂糖水にまじったので、ろ過してとりのぞくことにした
実験1について、砂糖水を3日間そのままにしておいたあとのモデルを、左のア~エから1つ選びなさい。
図の・は、目に見えないほど小さな砂糖の粒子を表す。
↓解答解説↓
- ウ
→溶質の粒子は均一に散らばり、放置しても沈まない性質だから覚えておこう
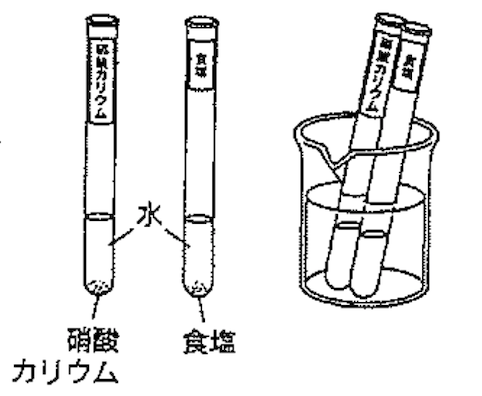
- 硝酸カリウム、食塩をそれぞれ3gずつ試験管に入れ、5gの水(20°C)を加えて溶かす。
- 80°Cくらいの湯を用意して、試験管を湯につけ、硝酸カリウムと食塩を溶かす。
- ②の水溶液を別の試験管に約2mLとって水で冷やす。
溶けきらないものは、上澄みの部分を約2mlとって冷水で冷やす。 - ③で溶質が現れたら、ろ過して固体を分け、得られた固体のようすを観察する。
- ③で溶質が現れなければ、試験管の中の水溶液をスライドガラスの上に1滴たらし、水を蒸発させてようすを観察する。
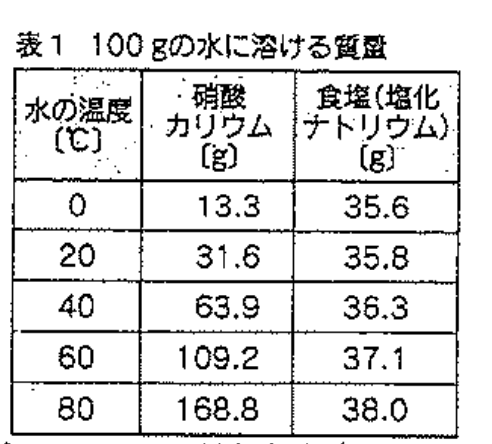
(1) ①で,①硝酸カリウムと②食塩を入れた試験管に、それぞれ溶け残りはあるか、ないか。表1をもとに答えなさい。
(2) ②で、①硝酸カリウムと②食塩を入れた試験管に、それぞれ溶け残りはあるか、ないか。
(3) ④で、片方の試験管から針状の固体が得られた。この固体は硝酸カリウム・食塩のどちらか。
(4) 5で、食塩水の水分を蒸発させるとどうなりますか。
(5) ①硝酸カリウムと、②食塩の溶け方は、それぞれのア・イのどちらと考えられますか。
ア決まった量の水に溶ける最大の量が、温度によってあまり変わらない。
イ決まったの水に溶ける最大の量が、温度によってちがう
↓解答解説↓
- ある
- ある
- ない
- ある
- 硝酸カリウム
- 白い固体が現れる
- 1ーイ 2ーア
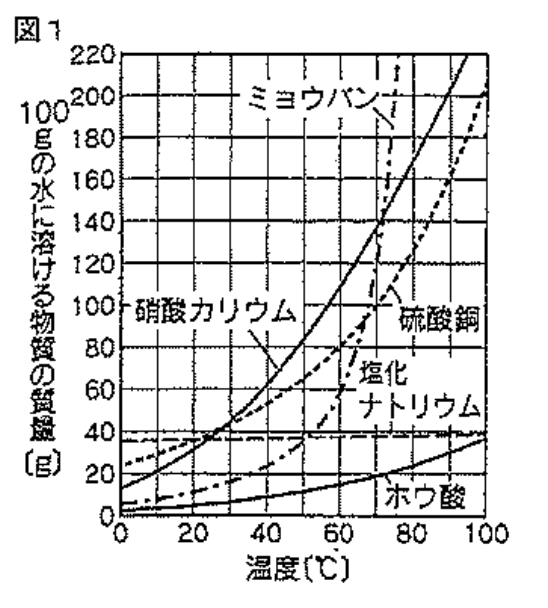
(1)図1のグラフから、20°Cの水100gに塩化ナトリウムとミョウバンをそれぞれ40g加えたとき、溶け残りが多いのはどちらか。
(2) ①0°Cのときと、②60°Cのとき、それぞれ溶ける量が多いのは硝酸カリウム・塩化ナトリウムのどちらか。
(3) 塩化ナトリウムの溶解度の特徴を「温度」という言葉を使って書きなさい。
↓解答解説↓
- ミョウバン
- 1ー塩化ナトリウム 2ー硝酸カリウム
- 温度が変わっても溶解度があまり変化しない
塩化ナトリウムは温度が高くなっても横線のグラフになっているのに注目しよう
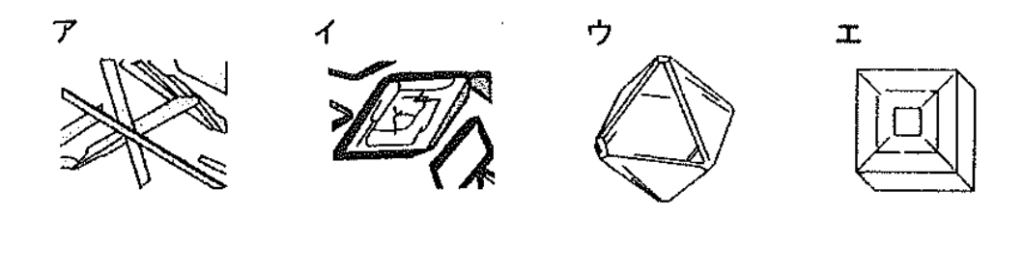
次の図ア~エは、それぞれ硝酸カリウム、塩化ナトリウム、硫酸銅、ミョウバンのどれか答えよう
↓解答解説↓
- アー硝酸カリウム イー硫酸銅 ウーミョウバン エー塩化ナトリウム
物質の溶け方とろ過の方法まとめ
記事のまとめ
次は状態変化と上流について見ていこう
これだけ覚えて点数アップ!中学1年理科10物質の状態変化と蒸留テスト対策問題